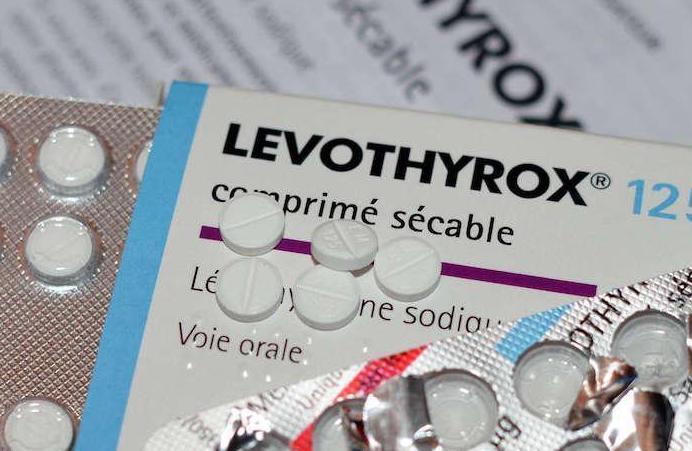
Depuis le changement, fin mars, de la formule du Levothyrox par le laboratoire Merck (à la demande de l'ANSM), 17 310 patients ont fait part d’effets indésirables pénibles ou insupportables, sur les 2,3 millions qui prennent la nouvelle formule.
Pour mémoire, ce changement de formule ne concerne que les « excipients », les produits inertes du comprimé, et visait à répondre à une demande de l’Agence du Médicament qui voulait assurer la stabilité du médicament. L’ANSM a publié le point d’enquête sur la période allant de fin mars au 15 septembre 2017 ont été publiés le 10 octobre 2017. D'autres études, toxicologiques en particulier restent en cours. L'ANSM n'explique pas la fréquence des plaintes.
Une enquête nationale
Une enquête nationale de pharmacovigilance a été initiée par l’ANSM lors de la mise à disposition de la nouvelle formule de Levothyrox en mars 2017, afin d’analyser les signalements d’effets indésirables rapportés. Les premiers résultats de cette enquête portant sur la période allant de fin mars au 15 septembre 2017 ont été publiés le 10 octobre 2017.
La poursuite de l’enquête réalisée sur la période du 15 septembre au 30 novembre 2017 sur la base des cas enregistrés dans la base nationale de pharmacovigilance (BNPV) confirme que les effets indésirables rapportés avec le Levothyrox nouvelle formule sont similaires en type et en gravité à ceux du Levothyrox ancienne formule.
Une fréquence inhabituelle
Sur la période du 15 septembre au 30 novembre 2017, 12 248 cas d’effet indésirables ont été enregistrés dans la base nationale de pharmacovigilance (BNPV). Ils ont été analysés, en complément des 5 062 cas déjà analysés dans la période de fin mars au 15 septembre 2017. Ces cas ont été très majoritairement déclarés par les patients (90 %).
Le portail de pharmacovigilance de l’ANSM a joué son rôle : dès que les patients ont appris par la presse qu’ils leur était possible de déclarer leurs effets indésirable, le nombre de signalement a bondi : il a été multiplié par 80 en quelques jours et la part des signalements par les patients est passée de 5% en temps normal à plus de 90%.
Globalement, sur l’ensemble de ces deux périodes étudiées dans le cadre de l’enquête de pharmacovigilance, le pourcentage de patients signalant des effets indésirables avec le Levothyrox est estimé à 0,75% des patients traités (2,3 millions de patients).
Des effets habituels
Les effets indésirables les plus fréquemment rapportés dans les plaintes sont : fatigue, maux de tête, insomnie, vertiges, dépression, douleurs articulaires et musculaires, perte des cheveux. Ces effets étaient déjà rapportés avec le Levothyrox ancienne formule avec cependant une fréquence inédite et inattendue.
Depuis le début de l’enquête de pharmacovigilance, 19 décès ont été rapportés et analysés, mais il n’a pas pu être établi de lien avec la nouvelle formule de Levothyrox.
Un cas de suicide rapporté a conduit à une analyse approfondie de 79 cas de troubles à type d’idées suicidaires sur la période. Les données issues des cas ne sont pas suffisamment complètes pour permettre d’établir un lien entre les effets indésirables de troubles psychiatriques avec la nouvelle formule de Levothyrox d’après l’ANSM.
Une liaison temporelle
Parmi l’ensemble des cas déclarés, 4030 cas comportent une information sur le bilan thyroïdien, dont 1745 cas sont documentés vis-à-vis de la chronologie de prise de Levothyrox nouvelle formule et des valeurs de TSH renseignées avant ou après le changement de formule de Levothyrox. Ces 1745 cas ont fait l’objet d’une analyse détaillée. Cette dernière confirme la survenue possible (chez environ 1/3 des cas analysés) de déséquilibres thyroïdiens lors du passage de Levothyrox ancienne formule au Levothyrox nouvelle formule.
Discordance effets secondaires et déséquilibre thyroïdien
L’analyse montre également que 2/3 des patients qui déclarent des effets indésirables ont des dosages de TSH dans les normes attendues. Le profil d’effets indésirables est similaire chez tous les patients qu’ils soient en hypothyroïdie, en hyperthyroïdie ou avec une TSH dans les normes attendues.
L’analyse de l’ensemble des cas ne permet pas la mise en évidence de nouveaux effets indésirables avec le Levothyrox nouvelle formule, ni de facteurs explicatifs. Pourtant, il existe quelques pistes.
La nouvelle formule a-t-elle pu "empoisonner" les malades ?
Il faut attendre les analyse toxicologiques diligentées par l'ANSM et la Justice, mais sauf erreur du laboratoire Merck, cela paraît peu probable. Le mannitol et l’acide citrique qui ont remplacé le lactose ne peuvent entraîner les manifestations décrites.
On les retrouve à des doses nettement plus élevées dans de nombreux aliments, notamment les bonbons et chewing-gums sans sucre sous les noms de code E421 et E330, ainsi que dans de très nombreux autres médicaments sans qu’aucun effet indésirable n’ait été rapporté.
Ces mêmes nouveaux comprimés de Levothyrox sont largement utilisés dans d’autres pays sans qu’aucun trouble n’ait été notifié.
Le dosage a-t-il pu être modifié ?
Il est certains que le dosage est différent. C'est même pour cela que l'ANSM a demandé le changement de formule : afin d'obtenir une stabilité des concentration de produit actif dans le temps. L'ancienne formule avait tendance à perdre en efficacité avec le temps. Tout changement de spécialité ou de formule peut modifier l’équilibre hormonal et nécessiter un réajustement du dosage qui peut prendre « un certain délai ».
Pour autant, est-ce que remplacer du lactose par du mannitol est sans aucun effet sur la pharmacologie du médicament. Probablement chez la majorité des malades, mais probablement pas pour certains d’entre eux. Un phénomène déjà connu car l’ANSM rappelle que, déjà, avec l’ancienne formule du Levothyrox, près de 15% des malades se plaignaient déjà d’effets indésirables à un moment donné ou l’autre de l’année.
Est-ce que l'effet de la L-thyroxine peut être modifiée ?
De nombreuses circonstances, qu'elles soient physiologiques, paraphysiologiques ou clairement pathologiques, peuvent altérer l'absorption de la lévothyroxine dans le corps humain.
L'absorption de lévothyroxine peut en effet être altérée par l'âge, le jeûne, l'ingestion de certains aliments (fibres alimentaires, raisins, soja, papaye et café) ou de certains médicaments (inhibiteurs de la pompe à protons, antiacides, sucralfate…).
De plus, de nombreuses maladies gastro-intestinales, telles que les celles qui perturbent l'intégrité de la barrière intestinale et les maladies qui altèrent l'acidité naturelle de l’estomac, peuvent diminuer l’apport réel en lévothyroxine.
La TSH est-elle un mauvais examen pour évaluer l'état des malades ?
La TSH ultra-sensible est l'examen de référence à l'international pour évaluer l'efficacité d'un traitement substitutif en L-thyroxine. Est-il pour autant parfait ? Pas forcément pour ce qui concerne la mesure de l'impact sur différents organes, dont le cœur. Une étude récente révèle ainsi que la Thyroxine libre (FT4) serait meilleure pour évaluer l'impact sur le cœur. D’après les auteurs, la TSH serait en réalité plus un marqueur des effets hypophysaires des hormones thyroïdiennes, alors que la thyroxine-libre, qui est convertie en triiodothyronine, serait plutôt un effecteur avec une action directe sur les organes-cibles, dont le cœur, et donc un meilleur marqueur de l'effet final.
Poursuite des investigations
Les données de cette enquête de pharmacovigilance continueront à être analysées au regard de différentes investigations complémentaires. En effet, dans le cadre de la surveillance des spécialités à base de lévothyroxine, l’ANSM a lancé en octobre 2017 une étude de pharmaco-épidémiologie sur la base des données de l'Assurance Maladie. Les résultats du volet descriptif sont prévus au premier trimestre 2018. En complément, une enquête de pharmacovigilance sur les effets indésirables des autres médicaments à base de lévothyroxine disponibles depuis octobre 2017 est également en cours. Une analyse des premiers résultats est attendue au 1er semestre 2018 de manière à disposer de données suffisantes.
Dans Pourquoi Docteur, le Pr Jean-François Bergmann évoquait, en sus des déséquilibres hormonaux induits par le changement de formule, un effet nocebo et l'effet amplificateur des réseaux sociaux qui ont servi de caisse de résonance dans une spirale collective totalement disproportionnée.
Au final, le plus important c'est que des malades souffrent. Heureusement, la mise à disposition de plusieurs alternatives thérapeutiques a permis à 2/3 d’entre eux d’améliorer leur qualité de vie. Il reste à trouver une solution pour les autres. La restauration d'un climat de confiance ne se fera que par la transparence des données analysées. L'ANSM doit continuer comme cela.
Le numéro vert d’information (0.800.97.16.53 ) est accessible du lundi au vendredi de 9 heures à 19 heures pour répondre aux questions des patients.
Pour déclarer tout effet indésirable : www.signalement-sante.gouv.fr