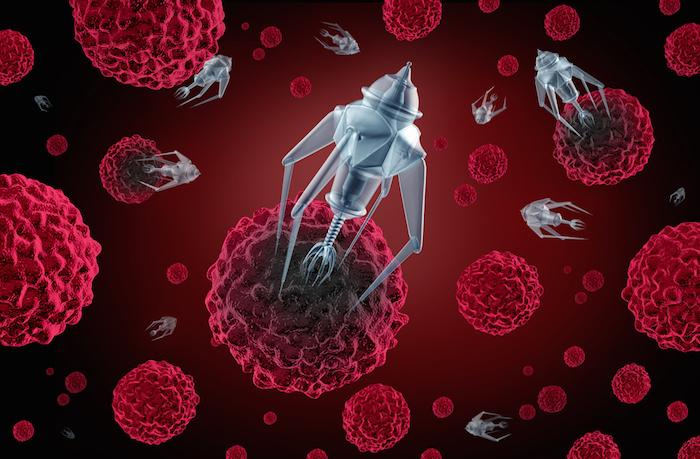
Les scientifiques ont programmé avec succès des nanorobots pour faire rétrécir les tumeurs en interrompant leur approvisionnement en sang. La thrombine (protéine de la coagulation sanguine) peut bloquer le flux sanguin tumoral en coagulant le sang dans les vaisseaux qui alimentent la croissance tumorale. Ainsi une sorte mini-crise de cardiaque est provoquée, entraînant la mort du tissu tumoral.
Le premier système robotique à ADN autonome
Les chercheurs ont conçu le premier système robotique à ADN entièrement autonome vecteur d’un design très précis de thérapie ciblée anti-cancéreuse. Les résultats de leur étude, portant sur l’utilisation de cette technologie sur des mammifères murins (genre de chauves-souris) atteints de cancer du sein, de l’ovaire, du poumon ou de mélanome, ont été publiés le 12 février 2018 dans Nature Biotechnology. La nouvelle technologie mise au point pourrait à l’avenir être déclinée à plusieurs formes de cancers puisque toutes les tumeurs solides étant alimentées par des vaisseaux sanguins sont essentiellement similaires.
Une thérapie "nanociblée"
Jusqu’alors, le défi résidait dans le fait de concevoir et contrôler des nanorobots ciblant des tumeurs cancéreuses afin de les détruire sans altérer aucune cellule saine. L’équipe internationale de chercheurs a surmonté cet obstacle en utilisant une stratégie apparemment simple : cibler très sélectivement les tumeurs et les "affamer". Initialement, les scientifiques souhaitaient interrompre l’approvisionnement sanguin tumoral en provoquant une coagulation sanguine efficace, en toute sécurité dans différents types de tumeurs solides, en utilisant des nanotransporteurs à base d’ADN.
Selon les chercheurs, les nanorobots peuvent être programmés pour véhiculer des charges moléculaires et provoquer des blocages sanguins au niveau des vaisseaux alimentant la tumeur, ce qui peut entraîner la mort des tissus et faire diminuer la taille de la tumeur. Chaque nanorobot mesure 90 sur 60 nanomètres. Une des enzymes-clés de la coagulation, la thrombine y est greffée. Cette dernière peut bloquer le flux sanguin approvisionnant la tumeur en coagulant le sang qui l’alimentent. Cela provoque une espèce de mini crise cardiaque qui entraîne la mort du tissu tumoral.
En pratique, le nanorobot est injecté en intra-veineuse et migre vers la tumeur. Le défi consiste à le programmer afin qu’il attaque uniquement les cellules cancéreuses. Pour ce faire, les chercheurs ont intégré au nanorobot un aptamère d’ADN, un oligonucléotide synthétique capable de fixer un ligand spécifique voire de catalyser une réaction chimique sur ce ligand. Ce système pourrait spécifiquement cibler une protéine appelée "nucléoline" qui est produite en grande quantité uniquement à la surface des cellules endothéliales tumorales. Une fois fixé à la surface du vaisseau sanguin tumoral, le nanorobot, de par sa programmation, libèrant la thrombine au cœur de la tumeur.
Des résultats prometteurs
En termes de résultats, les scientifiques ont obtenu une réduction des tumeurs immunologiquement inerte, notamment chez les souris, n’altérant aucunement la coagulation sanguine physiologique ou la morphologie cellulaire. Par ailleurs, aucun effet indésirable telle qu’une propagation cérébrale qui aurait pu provoquer un AVC n’a été constaté. Les nanorobots ont bloqué l’apport sanguin tumoral, provoquant des lésions tissulaires tumorales dans les 24h après leur injection, sans altérer les tissus sains. L’organisme les a ensuite éliminés "naturellement".
48h plus tard, on pouvait détecter des signes de thrombose avancée et au bout de 3 jours des thrombi dans tous les vaisseaux tumoraux. L’étape clé est de libérer la thrombine uniquement lorsqu’elle est localisée au sein des vaisseaux sanguins tumoraux. En pratique, sur le modèle murin de mélanome, 3 souris sur 8 ont montré une régression complète de la tumeur, le temps de survie ayant par ailleurs plus que doublé, passant de 20,5 jours à 45 jours. Le test du système sur un modèle murin de cancer de poumon a montré un rétrécissement des tissus tumoraux après deux semaines de traitement.
Cette nouvelle technologie permet de nourrir de nombreux espoirs car le nanorobot a, en plus d’affecter la tumeur primaire, empêché la formation de métastase. Par ailleurs en modifiant la géométrie des nanostructures et leurs cargaisons, on peut imaginer décliner ce concept à d’autres pathologies.