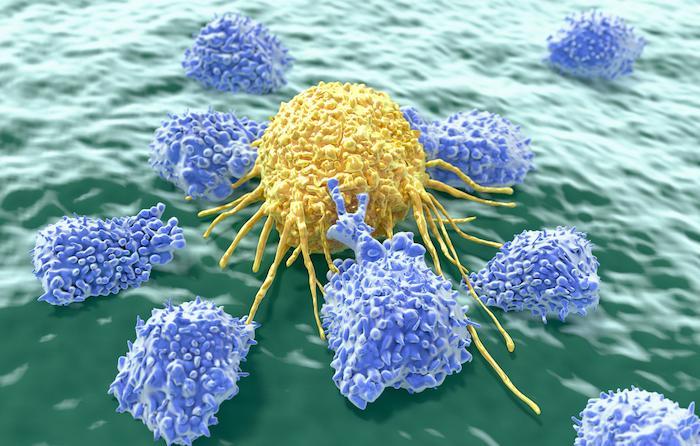
Les lymphomes B diffus à grandes cellules qui sont réfractaires aux traitements de 1ère et de 2e ligne, ou qui rechutent après une greffe de cellules souches, ont un très mauvais pronostic.
Dans la plus large étude à ce jour (93 malades), le tisagenlecleucel, un lymphocyte T génétiquement modifié pour attaquer une protéine à la surface des cellules lymphomateuses, donne une réponse dans 52% des cas. Quarante pour cent des malades ont une réponse complète et 12% ont une réponse partielle. Les patients inclus avaient déjà reçu au moins deux lignes de traitement. Cette étude JULIET est publiée dans le New England Journal of Medicine.
Des résultats étonnants
Soixante-cinq pour cent malades souffrant de lymphome B diffus à grandes cellules, recrutés dans le monde entier, sont sans rechute un an plus tard, dont 79% ont une réponse complète. Au terme de cette étude, la survie médiane sans progression des patients n'a pas été atteinte.
Ces résultats se comparent avantageusement aux études antérieures dans les lymphomes B diffus à grandes cellules avec la chimiothérapie. L'étude SCHOLAR-1, publiée en 2017, avait révélé que seulement 7% des malades souffrant de lymphome B diffus à grandes cellules réfractaire avaient une réponse complète. La survie globale médiane n'était que de 6,2 mois.
Des données antérieures de cet essai JULIET ont conduit à l'approbation par l’agence du médicament américaine (FDA) du tisagenlecleucel, le 1 er mai 2018, pour le traitement des malades souffrant de lymphome B diffus à grandes cellules. Ces nouveaux résultats témoignent d’un bénéfice de ce traitement sur le long terme.
Une complexité du processus
Le processus de préparation du traitement est compliqué et c’est pour cela qu’il était important d’en tester la faisabilité au niveau mondial. L'équipe de soins en hématologie prélève le sang du malade et en extrait les lymphocytes T (avant de réinjecter le sang). Les lymphocytes T de chaque malade sont ensuite expédiés dans le laboratoire de Novartis, à Morris Plains, au Etats-Unis. Les lymphocytes T de chaque malade y sont génétiquement modifiés afin d’exprimer un anticorps de surface anti-CD19, capable de cibler les cellules B responsables de la maladie, cellules qui ont une protéine de surface appelée CD19, et de les détruire très efficacement : comme il s’agit de cellules vivantes, la destruction est plus efficace qu’avec de simples anticorps.
Puis les cellules T modifiées, les « CAR-T cells », sont multipliées et sont retournées à l'hôpital et réinjectées au malade. Chaque cellule est ainsi compatible avec le malade dont elle est issue, elle n’est pas détruite par le système immunitaire et elle reste capable de se multiplier rapidement, produisant des millions de cellules-filles dotées des mêmes caractéristiques anti-CD19. Celles-ci vont attaquer violemment les cellules lymphomateuses porteuses du CD19 et entraîner leur destruction spécifique.
Une forme d’immunothérapie
Il s’agit donc bien d’une forme d'immunothérapie, une autogreffe de lymphocytes T modifiés, qui vont détruire spécifiquement les cellules cancéreuses CD19, où qu’elles soient dans le corps et sans nécessité d’une chimiothérapie. Mais la destruction en masse de ces cellules cancéreuses peut avoir des effets secondaires potentiellement graves mais généralement limités dans le temps (phase aiguë).
L'effet indésirable le plus fréquent est le syndrome de libération de cytokines (58%), qui provoque des symptômes graves tels que fièvre, œdème et hypotension, avec éventuellement des effets neurologiques, tels qu’un délire, mais les médecins ont appris à gérer ces effets secondaires en unité de greffe en hématologie (anti-IL6). Aucun décès dans cet essai n'a été attribué au traitement réalisé.
Des résultats jamais vus
« La survie sans progression médiane n'a pas été atteinte pour les répondeurs complets », ont écrit les auteurs. La probabilité de survie à 12 mois « est de 90% chez les répondeurs complets ».
« Dans l'ensemble, c'est extrêmement excitant », a déclaré Michael Bishop, l’un des auteurs de l’étude « car les rechutes après 12 mois sont rares. Notre première patiente, traitée en mai 2016, est de retour au travail depuis deux ans et demi. Cet essai démontre que le traitement par les CAR-T cells peut fournir un taux élevé de réponses durables ».
L’approbation de tisagenlecleucel par la FDA chez les patients atteints de DLBCL récidivant ou réfractaire est basée sur cet essai clinique de phase 2 JULIET. C’est la plus grande étude internationale portant sur un traitement CAR-T cell dans le lymphome B diffus à grandes cellules.