- Contenant un principe actif appelé acétate de cyprotérone, l’Androcur et ses génériques sont prescrits aux femmes souffrant d’hirsutisme, contre l’acné, l’endométriose ou en guise de contraception. Les hommes souffrant d'un cancer avancé de la prostate peuvent aussi s'en voir prescrire.
- En France, l'Agence du médicament a mis en place un numéro vert (0 805 04 01 10) accessible du lundi au vendredi de 9h à 19h" pour répondre aux questions des patients sous Androcur.
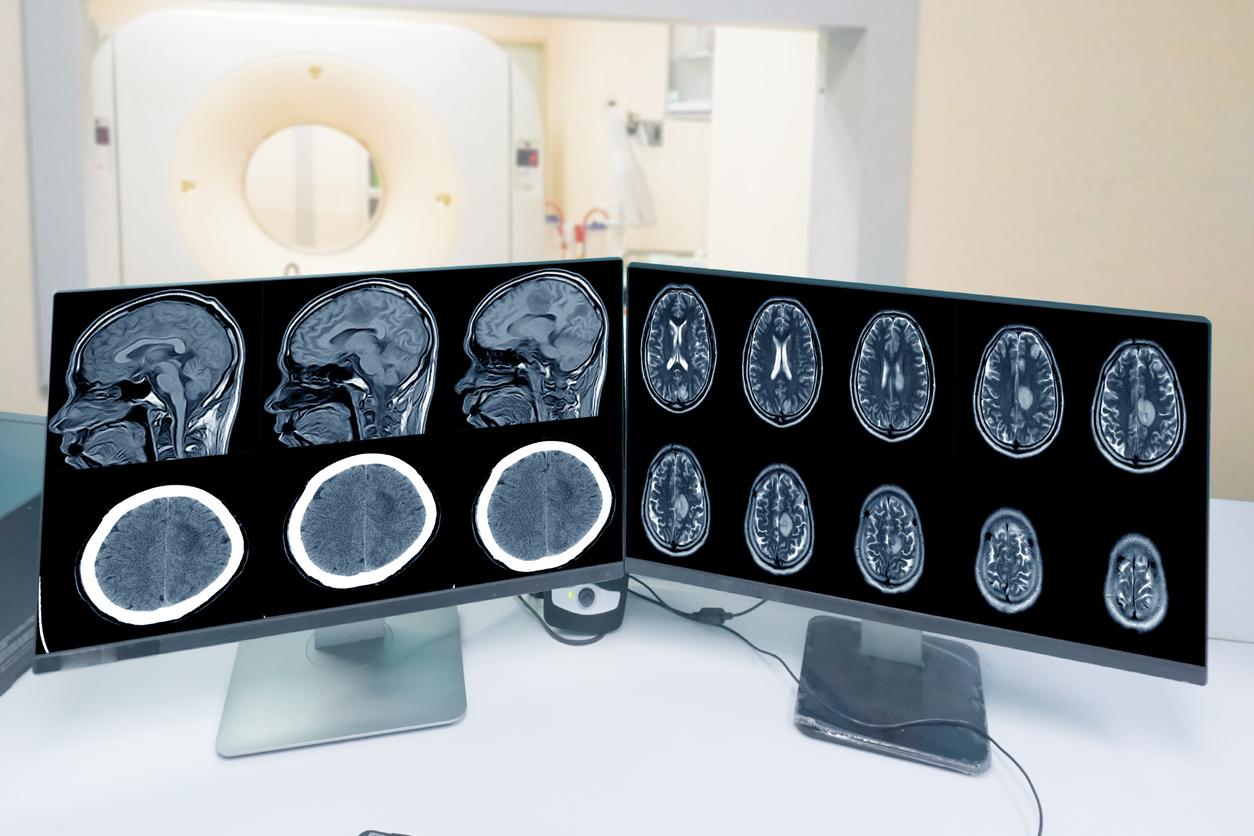
L’acétate de cyprotérone (CPA) est bien responsable de l’accroissement du risque de méningiome, une tumeur cérébrale généralement bénigne mais qui peut fortement impacter la qualité de vie en causant notamment un handicap lié à une compression du cerveau.
C’est la conclusion d’une nouvelle étude publiée dans Scientific Reports vendredi 4 février. Menée par des chercheurs de l’université de Bristol, en Angleterre, elle confirme les résultats d’autres travaux, notamment une étude de l’Assurance-maladie datant de 2018, et suspectait l’Androcur de multiplier jusqu'à 20 (après 5 années de traitement), et même plus, la probabilité de méningiomes chez les femmes traitées longtemps et à hautes doses.
Des méningiomes quand le médicament est utilisé à fortes doses
Commercialisé depuis les années 1980 par les laboratoires Bayer, l’Androcur est un progestatif prescrit pendant des années aux femmes souffrant d’hirsutisme, c’est-à-dire un développement extrême de la pilosité, mais aussi contre l’acné, l’endométriose ou en guise de contraception. Appartenant à la classe des antiandrogènes stéroïdiens et contenant un principe actif appelé acétate de cyprotérone, l’Androcur est aussi utilisé chez les hommes pour traiter le cancer de la prostate à un niveau avancé.
Dans ces nouveaux travaux, et compte tenu de l’utilisation répandue de l’acétate de cyprotérone, les chercheurs ont effectué une méta-analyse à partir de quatre études portant sur un total de 8 132 348 patients. L’objectif était d’évaluer si l’utilisation à forte dose de ce médicament était associée à l'incidence des méningiomes.
L'échantillon comprenait 165 988 patients identifiés comme prenant de l'acétate de cyprotérone à des doses variables. À l'aide de ces données, l'équipe a analysé l'apparition de méningiomes chez les patients utilisant de l'acétate de cyprotérone à forte dose par rapport à ceux utilisant de faibles doses. Une association significative entre l'utilisation de fortes doses et un risque accru de méningiome a bien été trouvé, ce qui n’a pas été le cas avec les faibles doses.
"La cause des méningiomes est controversée mais il existe des preuves solides suggérant un rôle plausible des hormones sexuelles dans l'apparition des méningiomes, souligne Keng Siang Lee, étudiant en médecine et auteur principal de l'étude. Nous savons qu'il a une prédilection pour les femmes, surtout après la puberté."
Une limitation des conditions d’utilisation en France et en Europe
À la lumière de ces résultats, les chercheurs rappellent que la prescription d’Androcur à forte dose, en particulier pour des indications hors AMM, doit être considérée avec prudence. Ils suggèrent également qu’un "dépistage systématique et la surveillance des méningiomes par IRM cérébrale" soient proposés aux patients à qui l'on prescrit de l'acétate de cyprotérone à des doses élevées et pendant de longues périodes.
C’est le cas en France. Depuis le 1er juillet 2019, tout nouveau patient débutant un traitement avec de l’Androcur ou un de ses génériques est systématiquement informé du risque de tumeur lié à son utilisation prolongée. Début 2020, l’Agence européenne du médicament (EMA) a également émis une série de recommandations pour limiter son utilisation. Désormais, il doit être utilisé uniquement dans les cas d’hirsutisme sévère où les autres traitements ont échoué. Son utilisation est maintenue dans le traitement du cancer de la prostate. En cas d’antécédent de méningiome, l’Androcur ne peut plus être utilisé même à faible dosage.
Pour l’heure, les chercheurs reconnaissent ne pas savoir si "l'acétate de cyprotérone en dessous d'un certain seuil peut être totalement sûr en termes de risque de méningiome" et souhaitent donc poursuivre les recherches cliniques sur le lien entre le médicament et le risque de méningiome intracrânien.