9 personnes sur 10 ne veulent pas savoir. Elles sont nées dans une famille à risque de maladie de Huntington et si l’un de leurs parents en est atteint, le risque est de 1 sur 2 pour qu’elles aient hérité du gène HD responsable de cette dégénération neurologique progressive qui provoque à partir de la quarantaine des mouvements brusques et incontrôlés ainsi que des troubles de la mémoire et de l’attention. Même si le test génétique existe, en l’absence de traitement contre la maladie de Huntington, ces personnes préfèrent très majoritairement continuer à vivre leur vie sans savoir si elles sont ou non porteuses du gène de cette maladie rare, qui touche 6000 personnes en France.
Ne pas savoir mais aider la recherche
« Mais beaucoup d’entre eux sont cependant prêts à aider à la découverte de traitements et le design de notre essai leur a permis de participer tout en respectant leur droit à ne pas vouloir connaître leurs informations génétiques personnelles », explique le Dr Diana Rosas, de l’Institut des maladies neurodégénératives du Massachusetts General Hospital. Cette chercheuse américaine et son équipe publient aujourd’hui dans la version en ligne de la revue Neurology les résultats d’un essai aussi prometteur sur le fond que sur la forme. Ils démontrent en effet qu’une supplémentation quotidienne de 30 grammes en créatine permet de ralentir l’atrophie des zones cérébrales touchées au début de la maladie de Huntington. Et pour la 1e fois, parmi les 64 participants à l’étude, 45 étaient des personnes à risque ayant refusé de faire le test génétique. Il a été pratiqué pour les besoins de l’étude mais les résultats n’ont pas été communiqués ni aux médecins qui conduisaient l'étude, ni aux personnes qui ne le souhaitaient pas.
Dans cet essai Precrest, les chercheurs ont voulu vérifier l’hypothèse créatine. Dans les cellules cérébrales des personnes malades, la huntingtine, une protéine-clé dans la production d’énergie cellulaire ne fonctionne pas correctement. Les chercheurs ont donc tenté de compenser ce dysfonctionnement grâce à la créatine, une protéine très impliquée dans l’apport d’énergie aux cellules musculaires.
L’atrophie du cerveau est visiblement ralentie
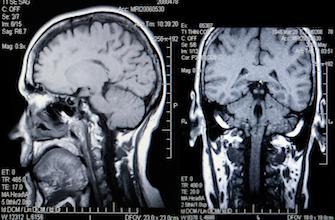
Pendant 6 mois, la moitié des personnes recevaient deux fois par jour un complément alimentaire à base de créatine, soit une dose maximum de 30g par jour et l’autre moitié un placebo. L’année suivante, tous ont pris le traitement à la créatine. Au début de l’étude, qu’ils aient fait le test génétique ou non, les personnes étaient toutes pré-symptomatiques, c’est à dire qu’aucun d’entre eux n’avait déclaré la maladie. Parmi les patients porteurs de la mutation Huntington, les IRM réalisé au début de l’étude, à 6 mois et à 1 an et demi ont permis d’observer un ralentissement de l’atrophie des régions du cortex cérébral et des ganglions de la base, qui sont connues pour être les premières zones du cerveau touchées par la maladie.
En revanche, le traitement à la créatine n’a pas montré de différences de performances dans les tests cognitifs. Mais selon les chercheurs, les signes cognitifs de la maladie sont trop subtils à ce stade très précoce pour être ainsi détectés. « Les résultats de cet essai suggèrent que la prévention ou le retardement des symptômes de la maladie de Huntington sont faisables, que les individus à risque peuvent participer aux essais cliniques, même s’ils ne veulent pas connaître leur statut génétique et que des biomarqueurs utiles pourraient être développés, grâce à la neuro-imagerie, pour aider à confirmer ces bénéfices thérapeutiques », explique le Pr Steven Hersch, co-auteur de cet essai.
Un précédent pour les maladies génétiques
Au cours des 1 an et demi de l’étude, 15 patients ont abandonné, y compris parmi ceux se sachant malades, en raison des effets indésirables gastro-intestinaux de la créatine ou du stress d’être quotidiennement rappelé à leur risque de maladie de Huntington. Mais le Pr Hersch souligne que le design de l’essai Precrest créé un précédent important pour les autres maladies génétiques en montrant que la recherche clinique peut coexister avec les préoccupations de préservation de l’intimité génétique et de l’autonomie du patient.